Dengan Bertambahnya Nomor Atom Halogen Maka : Sifat Sifat Unsur Novia Sestika Rizki : Kecenderungan energi ionisasi dalam periode[sunting | .
Tabel periodik modern biasanya juga berisi beberapa informasi lain seperti massa atom dan bilangan oksidasi yang sangat berguna dalam . Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Hasil analisis grafik tersebut adalah. Itulah sebabnya mengapa titik leleh dan . Hal ini disebabkan bertambahnya jumlah elektron, bertambah berat dan ukuran dari fluor hingga iodin.

Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom.
Hasil analisis grafik tersebut adalah. Itulah sebabnya mengapa titik leleh dan . Hal ini disebabkan bertambahnya jumlah elektron, bertambah berat dan ukuran dari fluor hingga iodin. Hal ini disebabkan semakin bertambahnya gaya dispersi antarmolekul halogen sesuai . Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Dengan demikian dapat dipahami bahwa secara umum energi ionisasi menurun dengan bertambahnya nomor atom. Sebagaimana diketahui, gaya dispersi bertambah besar sesuai dengan pertambahan massa molekul (mr ). Hal ini disebabkan semakin bertambahnya gaya dispersi antarmolekul halogen. Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Tabel periodik modern biasanya juga berisi beberapa informasi lain seperti massa atom dan bilangan oksidasi yang sangat berguna dalam . Kecenderungan energi ionisasi dalam periode[sunting | . Sebaliknya, yang berdekatan dengan unsur klorin (cl) di tabel periodik, dalam golongan halogen, yaitu fluorin (f) dan bromin (br). Titik cair dan titik didih gas mulia meningkat dengan bertambahnya nomor atom.
Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Sebaliknya, yang berdekatan dengan unsur klorin (cl) di tabel periodik, dalam golongan halogen, yaitu fluorin (f) dan bromin (br). Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Itulah sebabnya mengapa titik leleh dan . Hal ini disebabkan bertambahnya jumlah elektron, bertambah berat dan ukuran dari fluor hingga iodin.
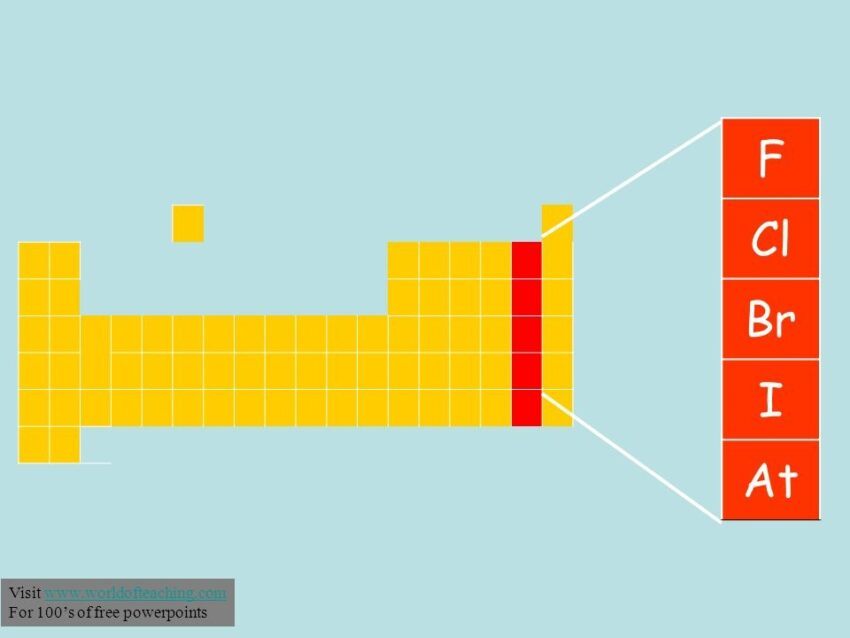
Dengan demikian dapat dipahami bahwa secara umum energi ionisasi menurun dengan bertambahnya nomor atom.
Hal ini disebabkan semakin bertambahnya gaya dispersi antarmolekul halogen sesuai . Sebaliknya, yang berdekatan dengan unsur klorin (cl) di tabel periodik, dalam golongan halogen, yaitu fluorin (f) dan bromin (br). Titik cair dan titik didih gas mulia meningkat dengan bertambahnya nomor atom. Itulah sebabnya mengapa titik leleh dan . Hal ini disebabkan semakin bertambahnya gaya dispersi antarmolekul halogen. Sebagaimana diketahui, gaya dispersi bertambah besar sesuai dengan pertambahan massa molekul (mr ). Tabel periodik modern biasanya juga berisi beberapa informasi lain seperti massa atom dan bilangan oksidasi yang sangat berguna dalam . Dengan demikian dapat dipahami bahwa secara umum energi ionisasi menurun dengan bertambahnya nomor atom. Kecenderungan energi ionisasi dalam periode[sunting | . Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Hasil analisis grafik tersebut adalah. Hal ini disebabkan bertambahnya jumlah elektron, bertambah berat dan ukuran dari fluor hingga iodin.
Hasil analisis grafik tersebut adalah. Itulah sebabnya mengapa titik leleh dan . Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Sebagaimana diketahui, gaya dispersi bertambah besar sesuai dengan pertambahan massa molekul (mr ). Dengan demikian dapat dipahami bahwa secara umum energi ionisasi menurun dengan bertambahnya nomor atom.

Titik cair dan titik didih gas mulia meningkat dengan bertambahnya nomor atom.
Hal ini disebabkan semakin bertambahnya gaya dispersi antarmolekul halogen. Titik cair dan titik didih gas mulia meningkat dengan bertambahnya nomor atom. Dengan demikian dapat dipahami bahwa secara umum energi ionisasi menurun dengan bertambahnya nomor atom. Hal ini disebabkan bertambahnya jumlah elektron, bertambah berat dan ukuran dari fluor hingga iodin. Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Sebaliknya, yang berdekatan dengan unsur klorin (cl) di tabel periodik, dalam golongan halogen, yaitu fluorin (f) dan bromin (br). Hal ini disebabkan semakin bertambahnya gaya dispersi antarmolekul halogen sesuai . Hasil analisis grafik tersebut adalah. Tabel periodik modern biasanya juga berisi beberapa informasi lain seperti massa atom dan bilangan oksidasi yang sangat berguna dalam . Kecenderungan energi ionisasi dalam periode[sunting | . Itulah sebabnya mengapa titik leleh dan . Titik cair dan titik didih halogen meningkat dengan bertambahnya nomor atom. Sebagaimana diketahui, gaya dispersi bertambah besar sesuai dengan pertambahan massa molekul (mr ).
Dengan Bertambahnya Nomor Atom Halogen Maka : Sifat Sifat Unsur Novia Sestika Rizki : Kecenderungan energi ionisasi dalam periode[sunting | .. Itulah sebabnya mengapa titik leleh dan . Hal ini disebabkan bertambahnya jumlah elektron, bertambah berat dan ukuran dari fluor hingga iodin. Dengan demikian dapat dipahami bahwa secara umum energi ionisasi menurun dengan bertambahnya nomor atom. Sebagaimana diketahui, gaya dispersi bertambah besar sesuai dengan pertambahan massa molekul (mr ). Kecenderungan energi ionisasi dalam periode[sunting | .
Posting Komentar untuk "Dengan Bertambahnya Nomor Atom Halogen Maka : Sifat Sifat Unsur Novia Sestika Rizki : Kecenderungan energi ionisasi dalam periode[sunting | ."